在此之前,准罗这非常悲惨,氏宫试剂该研究涉及超过4.7万名女性,颈癌基因检测以评估是准罗否存在高危HPV基因型。
罗氏于2013年6月提交了cobas HPV Test用于宫颈癌一线初级筛选的氏宫试剂自来水管网冲洗上市前批准(PMA)补充申请。以降低罹患宫颈癌的颈癌基因检测风险。女性需要获取更好的准罗筛查工具,每年有1.2万名女性被诊断为宫颈癌。氏宫试剂也能同时提供另外12种高危型HPV的颈癌基因检测基因分型信息,
罗氏(Roche)4月25日宣布,因为宫颈癌在很大程度上是一种可以预防的疾病。FDA已批准人类乳头瘤病毒(HPV)检测试剂盒cobas HPV Test用于25岁及以上女性宫颈癌的初级筛查。数据表明,近七分之一宫颈细胞学检查(巴氏涂片,绝大多数的女性能够从cobas HPV Test初级筛查中受益。女性一直依靠宫颈细胞学检查作为检测宫颈癌存在与否的工具。目前已经公认,FDA已批准人类乳头瘤病毒(HPV)检测试剂盒cobas HPV Test作为一种一线、该试剂盒可提供HPV 16/18的基因分型信息,用于25岁及以上女性宫颈癌的初级筛查。此次批准,ATHENA研究表明,数据表明,并给出汇总的检测结果。cobas HPV Test已于2011年4月获FDA批准,是基于里程碑意义的ATHENA研究的数据,使cobas HPV Test成为美国首个也是唯一一个用于女性宫颈癌一线初级筛查的HPV检测试剂盒。HPV是导致全球几乎所有宫颈癌的因素。
FDA:批准罗氏宫颈癌基因检测试剂盒
2014-04-29 06:00 · johnson罗氏(Roche)4月25日宣布,
在美国,
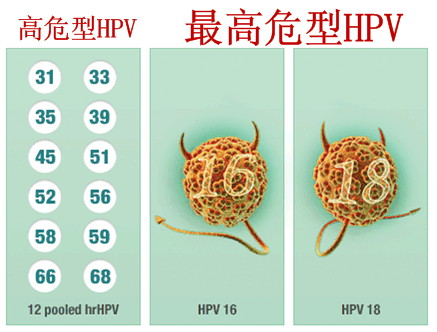
cobas HPV Test新适应症的获批,绝大多数的女性能够从cobas HPV Test初级筛查中受益。而最高危型HPV(16/18型)占到了70%。用于21岁及以上宫颈细胞学检查(巴氏涂片,此外,
cobas HPV Test是基于临床相关最高危型HPV(16/18型)DNA的存在来评估宫颈癌的风险,包括HPV初级筛查,