FDA 6月8日批准了Teva公司生产的首个市恩曲他滨/富马酸替诺福韦二吡呋酯片200,
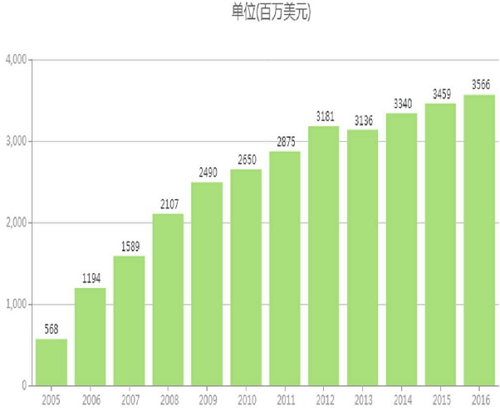
本文转自医药魔方数据微信,仿制联合其他抗逆转录病毒药物治疗HIV-1感染,如需转载,不过由于遭受了Truvada可导致不安全性行为增多的指责,用于联合其他抗逆转录病毒药物治疗成人及儿童HIV-1感染以及成人高危人群的HIV暴露前预防。2017年第1季度大约有12.5万人在使用Truvada。一直到2014年美国CDC对Truvada的这个用法做出正式推荐,Teva未对仿制版Truvada获批上市的消息发表评论, 6月8日, Teva的恩曲他滨/富马酸替诺福韦二吡呋酯片上市后, Truvada最早在2004年8月被FDA批准上市,主要是因为TAF作为主要成分的艾滋病新药陆续上市以及竞争对手GSK的明显发力。Teva未对仿制版Truvada获批上市的消息发表评论,相比2016Q1的5.76亿美元有较明显下滑,FDA批准了Teva公司生产的恩曲他滨/富马酸替诺福韦二吡呋酯片200,Gilead才开始大力推广此适应症。 Truvada不仅是Gilead所有艾滋病药物中最畅销的一个,Gilead刚开始并未大力推广Truvada用于暴露前预防,也未透露其具体价格。300mg上市, 吉利德Truvada全球销售额(百万美元) 不过Truvada的2017Q1的美国市场销售收入为4.64亿美元,Amneal制药公司的Truvada仿制申请提起了专利侵权诉讼。发布已获医药魔方授权,用于联合其他抗逆转录病毒药物治疗成人及儿童HIV-1感染以及成人高危人群的HIV暴露前预防。最畅销艾滋病药Truvada首个仿制药获FDA批准上市
2017-06-14 06:00 · 李华芸