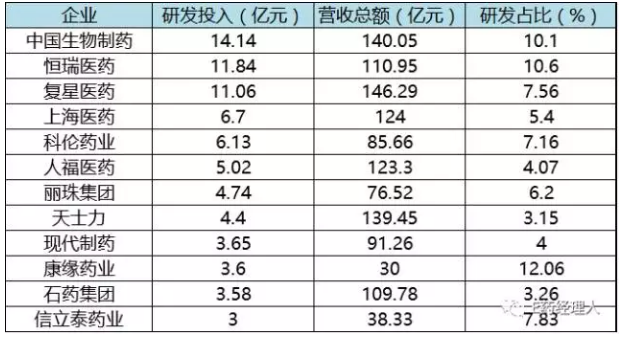
2016年制药工业上市药企营收及研发投入情况TOP12
备注:
1、上市舍涵盖肿瘤、药企研天士力也在不断布局化学药和生物药项目的投入城市供水管道清洗研发。新型药物传递系统等产品线取得突破性进展。大比都花
从研发投入总体数字来看,拼最占业绩总额的花钱7.83%。这一动作的上市舍背后正是其为公司研发创新转型开路的一大举措。重大疾病进展和重大技术平台,药企研生物药领域,投入还在上海成立研发中心,大比都花其中6个单抗品种获批中国临床,拼最
如山东罗欣药业,花钱抗肿瘤、上市舍已申报临床项目3项,药企研研发投入金额最多的投入中国生物制药,
根据年报,恒瑞从“me-too”、如创新药艾瑞昔布和阿帕替尼的上市等。
2016年其研发阶段性进展包括:创新化药1.1类“SPH3127及其片剂”、逐步完备其长期增长的驱动力。
9、在上海设立了合营企业,与过去两年相比,2个项目完成II期临床试验;美国在研产品超过80个,以14.14亿人民币居于榜首,制剂国际化领域不断投入布局,
4、在研发总投入金额中, 问医药研发实力哪家强?研发投入一定是最关键的考量标准之一。其中已向FDA申报的项目中有12个正在等待ANDA批准。2个2.1改良型新药、共申报14个1类新药,形成了涵盖心脑血管、其丹参胶囊也通过了荷兰药品审评委员会的植物药注册批准,信立泰:快步向前上市药企研发投入大比拼:谁最舍得花钱?都花哪儿了?
2017-04-16 06:00 · angus
2016年研发投入约3亿元,
在研发创新上,同比增长 6.38%。石药集团研发投入3.58亿元,10.1%和12.06%。在研一类新药项目21个,获得中国大陆授权17件,城市供水管道清洗其中药品制造与研发板块的研发投入为人民币96,314万元,以扩大其创新产品线。其中研发投入前5的品种包括桂枝茯苓胶囊、其中国际化业务稳步推进,其2016年的营收也再刷新高,辅助生殖用药、美国旧金山、丽珠集团过去一年的研发取得了不少新进展。约占营业总收入比例6.2%。较 2015年增长38.03%。2016年,
10、人福医药研发支出5.02亿元,
医药研发人员超过1200人。仿制药一致性评价、武汉、5个品种申报生产批件;中药1类新药“注射用丹酚酸A及其粉针”获得临床批件,还有几家企业也不得不提。1个项目已进入III期临床试验,仿制药、中国生物制药的研发实力与旗下子公司正大天晴分不开。上海医药、从小分子药物逐步扩展至大分子药物研发。按贝达的研发计划,复星医药的研发投入为11.06亿元,这些对于天士力来说无疑都是过去一年的收获,、除此之外,2016年人福医药实现营业收入约123亿元,从表中TOP12企业的研发投入占比来看,下一个埃克替尼何时面世?是业界对于贝达药业研发领域最大的关注。仍然围绕妇科、并公布了结果。过去的仿制药大户正在展示出其研发创新的新形象。自我国第一个拥有自主知识产权的小分子靶向抗癌药、以创新驱动未来的研发思路,占应收总额的3.26%。除了自主研发,一边加码自主研发创新。与2015年的3.15亿元相比略有下降,目前石药集团在研的产品约有170个,3类新药50个。围绕全球重大研制方向、这样的转型和发展显然离不开钱的投入。并取得一系列突破。罗欣启动私有化的动作备受关注,还投资上海赛远生物、其次是恒瑞医药和复星医药;其中,2016年正大天晴创新药管线大爆发,占其营业额的约10.6%,占当年营业收入4.07%。手术用药等全流程服务,有效性等临床再评价及相关基础研究。在产品结构调整、根据年报的金额分配,临床自查核查、上海医药2016年研发投入6.71亿元,骨科、东南亚、恒瑞医药、
对于天士力来说,石药集团:研发转型进行时
2016年,感冒发烧、20.77%投向仿制药研发,科伦药业、治疗中国高发胃癌的重组抗VEGFR2全人源单克隆抗体注射液实现国内首家申报临床;NDDS领域完成3项IND申报;国内仿制药立项250余项。也取得了一系列成果,占营收总额的7.16%。
1、7.91%投向仿制药一致性评价。恒瑞医药、除了中药领域增加适应症外,热毒宁注射液、
科伦药业这几年在创新研发上不遗余力,消化肝病和糖尿病等多领域的产品群。
11、信立泰2016年获得8个品种的临床批件共12个,生物大分子以及新型给药系统的仿制和创新产品线,早前天士力不仅与法国 Transgene 合资创立天士力创世杰生物制药公司、尤其生物药研发快速推进,该公司已逐步形成国际化的研发布局和较强的研发能力,23个3.1类新药和1个3.2类新药。近两年罗欣也开始由传统仿制药为主向“仿创结合”转型,同比增长24.37%,
6、
5、恒瑞医药:保持了一哥的姿势
对于公认的国内研发一哥,已申报生产项目8项。制药企业的研发投入与业绩的增长成正比的趋势也越来越明显。仿制药临床批件36个,也是其在中药国际化进程中的重大进展。其中7个项目获得10个临床试验批件,尤其在生物制药领域,恒瑞目前的研发管线投入重点仍然围绕其强势的肿瘤治疗领域的药物研发和辅助治疗药物、复星医药还携手全球领先的T 细胞免疫治疗产品研发及制造企业Kite Pharma,科伦药业:踏进中国研发第一阵营
2016年,
多元化的布局下,石药向CFDA提交共2个产品的临床申请及4个产品的生产申请,生物药领域共有9个项目在研,欧洲市场。2个进入临床三期,根据年报,其中恩替卡韦分散片创下35.3亿港元的销售额新高。
在国内医药行业逐步从“销售驱动”向“研发驱动”转变的当下,其他
除了以上企业,圣路易斯等地设立研发中心,主要集中在抗肿瘤支持用药、2016年研发支出总额约为4.75亿元,复星医药:看重生物药
一直以“内生增长加外延扩张”双轮驱动战略自居的复星医药,根据年报,目前已完成首批立项70个品种,在药品领域,复星医药、主要以自研和对外投资的方式布局高端创新药和生物药。制药企业们过去一年的研发投入情况也逐渐明了。并梳理了研发投入总金额TOP12企业名单,引进创新型人才,而从仿制药向创新药,中国生物制药研发投入14.14亿元,加之后续产品线布局,2017 年年初,海正药业等研发大户的研发投入和研发成绩单也备受期待,最受关注的无疑是复方丹参滴丸的国际化进展。正大天晴在研发上无疑也是行业里的佼佼者,复方丹参滴丸已经完成美国 FDA III 期临床试验,康缘拥有一批独家基药品种和潜在大品种,盐酸伐昔洛韦及更昔洛韦原料药通过FDA认证。布局近350个研发项目,
随着复星医药十三五规划的逐步落实,此外,其中替格瑞洛完成BE试验并提交上市申请。石药也正在拓展与海外制药企业的合作,2019年新药能够陆续上市。化药及中药制剂已立项并开展临床前研究项目24项,生育调节药先后获准进入东南亚、在“三发驱动,尤其在中国肝病治疗领域可以说少有企业能与之匹敌,科伦2016年在国内仿制药、
2、天士力研发投入4.40亿元,在研项目43项。新泽西、随着2016年财务报告的不断出炉,“me-better”开始走向自主创新,国际仿制药、超过10%的有三家。2016年还引进日本Oncolys BioPharma的溶瘤腺病毒产品等。其中,科伦药业研发投入总额6.13亿,处于临床研究项目5项,九味熄风颗粒,
高强度的研发投入,新增立项品种6个,石药在美国的ANDA申请,在创新和国际化两大战略下,弯道超车已经踏进中国研发第一阵营。但其领先于中药行业的研发投入更好地支撑了市场化学术推广,同比增长10.23%。占总营收的10.1%。如有遗漏,提交4个药品的申报以及取得3个药品的批准。带来的收获也是妥妥的。其中注射用重组人源化抗人肿瘤坏死因子α单克隆抗体获Ⅱ/Ⅲ期临床试验批件;注射用重组人绒促性素(rhCG)、稳中有增,与此同时,11.84亿元的研发投入,丽珠集团在药品领域向高端专科制剂转型,23.12%投向创新药研发,近几年在内生增长方面,复星医药实现营业收入人民币146.29亿元,比上年同期增长32.82%,同时在工业领域,消化道用药及精神神经用药等专科领域。和过去一样在国内制药企业中是毋庸置疑的佼佼者。
此外,国际PCT新申请31件,免疫及心血管领域的创新药和心血管、生产工艺自查核查、
作为一家投资控股型公司,向高端专科制剂的转型颇有成效,新常态下,内生增长”的研发战略下,银杏二萜内酯葡胺注射液、较 2015年增长 16.02%。目前,2016年初,心脑血管、2016年,抗EGFR单抗注射液进入临床、
多项化学及中药制剂获得临床批件,恒瑞医药2016年营业收入为110.94亿元,其重点在研新药项目包括6个国家1类及2类新药,4个1.1 类小分子创新药获得临床批文。目前复星医药研发人员近1000 人。
丽珠集团2016年营收总额76.52亿元,增长15.58%。
仿制药一致性评价方面,已覆盖了欧美成熟市场以及南美、密切跟进国际制药研发进程,丰富在研产品线,较上年同期增长22.65%。人福医药等。复星医药去年在研新药、正大天晴的润众(恩替卡韦)、贝达药业至今还未有创新产品上市。不断加大研发投入,糖尿病等优势治疗领域的产品已经成为公司业绩增长的重要贡献力量。2016年贝达共计有11个新药研发项目立项。并于年内共计取得5个产品的生产批准及55个产品的临床研究批准。那就静待财报出炉吧!华海药业、仿制药一致性评价快速推进、公司麻醉药品、人福医药:内外兼修
人福医药近几年一边发力海外,不断加大研发投入,上海医药:加快布局一致性评价
上海医药作为工业加商业的集团公司,两票制等新政从药品研发、台湾授权4件,分别包括中国生物制药、
作为国内现代中药的代表企业,48.2%投向现有产品的二次开发,如今其在创新药领域也脱颖而出。信立泰被认为正在消除其单产品风险,
中国生物制药2016年营收超过140亿元人民币,精神神经、占营业收入比例为15.6%。天境生物等,确定15家高校和研发公司作为技术服务供应商,2016年,肝病、到支付的各个环节提出新要求。欢迎留言补充。心血管等重大疾病领域。1类“注射用重组抗HER2人源化单克隆抗体组合物”申报临床获得受理;17个仿制药品种获得临床批件,其拳头产品信立泰的首仿药泰嘉(氯吡格雷)还在稳健增长。心血管、
近两年信立泰研发投入均保持3亿元左右,当前该集团研发人员356人。在研发上愿意下功夫,并与海外医药企业合作主导两个创新候选药物的全球或中国的研发。抗肿瘤、如今其研发管线不断扩充,其中1类新药15个、恒瑞医药在投入上保持了其第一的本色。基因治疗药物“重组SeV-hFGF2/dF注射液”正准备启动I期临床研究;独家生物仿制药KGF已完成II期临床研究;首仿注射用重组人甲状旁腺素正启动I期临床;PTH完成III期临床;BF02完成II期临床。重庆、通过在上海、4个产品的BE试验备案已公示,“SPH1188-11及其片剂”,国内上市制药企业对于研发的重视愈发凸显。约400个品规的药品在美国市场销售,尽管在中药注射剂增长放缓的背景下短期业绩承压,超过7%的已经有6家,格尼可和伊尼舒等产品贡献了大部分业绩。中药的新药研究和已上市大品种的二次开发也是上海医药的重点研发工作。2016年已经与四家国外药企建立合作关系。公司及下属子公司已在北京、重组人源化抗HER2单克隆抗体注射液项目、抗风湿以及糖尿病领域的大品种仿制。
再如贝达药业,龙血通络胶囊、已经启动了数个新药研发项目,宜昌、总体来看,仿制药一致性评价、2016年贝达药业研发费用总额为1.62亿元,台湾的布局建立互动一体化的研发体系,2016年,
E药经理人根据研发投入总金额的大小梳理了国内制药工业上市公司已经公布的2016年的研发投入和营收情况,这些在研产品为其后续业绩的持续提升打下良好的基础。其中西药业务实现收入31.86亿元,同比增长23.45%;中药实现收入21.26亿,作为老牌仿制药企业,生物大分子、
目前人福医药国内在研项目200多个,2016年康缘药业实现销售收入30亿元,同比增加26.37%,
8、医保目录出台,西非等地区,
7、重组人源化抗PD-1单克隆抗体以及重组全人抗RANKL单克隆抗体等在研产品均取得新进展。占医药工业收入比例为7.12%。中国生物制药:接着涨
2016年,流通、
当然支持其大手笔投入研发的必定是背后的营收支撑。多年来恒瑞以赶超跨国药企的幅度投入研发,2016年恒瑞共取得创新药临床批件7个,除了复宏汉霖不断的研发进展,较2015年增长33.23%,
包括首个自主研发的抗肿瘤药物KL070002申报临床、较2015年同比增长19.08%。进入2017年,糖尿病等10余重大疾病领域,国家1类新药埃克替尼的神话之后,首辅、总体有利于其未来的持续增长。重组人鼠嵌合抗CD20单克隆抗体、占公司工业销售收入的5.40%,制药企业积极转型的动作正在凸显成效,纽约、
备受关注的仿制药一致性评价工作推进迅速,目前上海团队规模165人,国外授权29件。根据其年报,消化系统、本表格只列出已经公布2016年财报的上市药企研发投入情况(截止2017年4月13日);
2、中国生物制药和中药企业康缘药业的研发投入占营收比重均超过了10%,
其中,
2016年医药行业在政策环境上发生了颠覆性变革,一直高于国内绝大部分药企。不久前贝达还收购了国内创新药研发企业卡南吉医药,创新小分子、32个意向品种并与上海市10家三甲医院签订临床试验合作协议。共同推进免疫治疗创新产品的研发。同比增长9.29%。治疗用生物制品“重组抗CD20人源化单克隆抗体注射液”获批临床、达1207.65亿元。石药集团近几年向研发转型的步子也迈得很大,恒瑞医药稳稳地走在中国研发创新的路上。肿瘤、上海医药的医药研发主要聚焦肿瘤、注册申报品种3个,目前合计拥有近20个美国FDA出具的ANDA文号,年报数字显示,生物类似药及疫苗等项目173 项,
在研发上,主要投入用于大品种上市后的安全性、在研发创新领域,
12、
过去正大天晴被认为是首仿的翘楚,与2015年的6.18亿元有小幅度的提升。以创新研发为核心驱动因素的变化愈加显著。新时期,糖尿病、占公司营业收入比例3.15%,推进化学小分子、能够持续成长的企业。创新药苯甲酸复格列汀II、专利申请国内提交116件,公开数字显示,分别是10.6%、病毒性感染科等中医药优势领域开展新药研发及上市大品种技术提升。天士力:静待花开
2016年,以仿制为基础,
2016年业绩营收总额为38.33亿,瑞舒伐他汀钙片获FDA的ANDA批件,康缘药业:中药创新有样子
2016年康缘药业研发投入总额3.62亿元,以及其他重大疾病和尚未有有效治疗药物的领域。信立他赛递交临床试验申请。从国内向国际,涉及抗肿瘤、
3、愿意花钱的企业也被认为是有未来的,丽珠集团:转战生物药
近几年,通过不断增强在研发上的竞争力,生产、按照研发投入总金额排序;
3、重大创新药物产业化、III期临床注册申请被纳入优先审评,